Генная терапия, нацеленная на натрий, успешно устраняет хроническую боль
Ученые стремятся разработать эффективные, основанные на генах способы нарушения болевых сигналов, возникающих при хронических состояниях, в надежде, что это может значительно улучшить качество жизни без каких-либо негативных побочных эффектов.
Последнее многообещающее открытие было сделано в Центре исследования боли Колледжа стоматологии Нью-Йоркского университета (NYU), специалисты которого разработали новую таргетную терапию для облегчения боли, вызываемой сконструированным вирусом.
«Существует острая потребность в новых методах лечения боли, в том числе для онкологических больных с нейропатией, вызванной химиотерапией», — сказал Раджиш Кханна, директор центра и профессор молекулярной патобиологии.
«Наша долгосрочная цель — разработать генную терапию, которую могли бы получать пациенты, чтобы лучше лечить эти болезненные состояния и улучшать качество своей жизни».
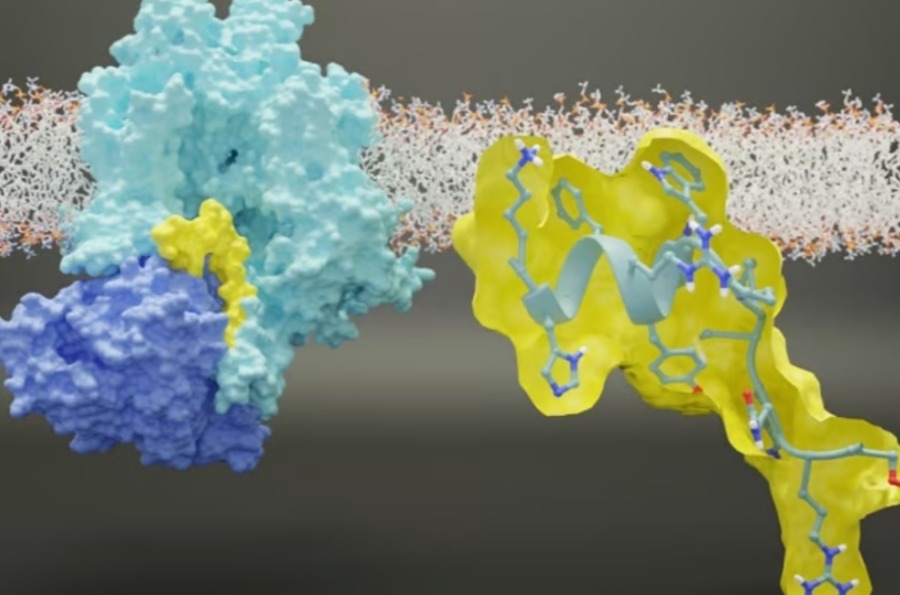
Что отличает их результаты, так это то, что они косвенно нацелены на натриевый канал NaV1.7, который находится на конце нервов, обнаруживающих боль, и до сих пор был в центре внимания многих исследований по борьбе с хронической болью. Вместо того, чтобы пытаться заблокировать натриевый канал, чтобы нарушить передачу сигналов по болевым нервам, ученые косвенно регулировали его с помощью белка, известного как CRMP2.
«Наше исследование представляет собой важный шаг вперед в понимании лежащей в основе биологии ионно-натриевого канала NaV1.7, который можно использовать для облегчения хронической боли», — сказал Кханна. «CRMP2 «разговаривает» с каналом ионов натрия и модулирует его активность, пропуская больше или меньше натрия в канал.
«Если мы заблокируем взаимодействие между Nav1.7 и CRMP2, запретив взаимодействие между ними, мы сможем уменьшить количество поступающего натрия», — добавил он. «Это успокаивает нейрон и смягчает боль».
Исследователи обнаружили область в канале NaV1.7, где CRMP2 связывается с ним, чтобы регулировать его активность. Интересно, что белок не связывался с другими ионно-натриевыми каналами, что позволяет предположить, что он обладает уникальной способностью нарушать этот путь для терапевтического использования.
«Это нас очень взволновало, потому что, если бы мы убрали этот конкретный фрагмент канала NaV1.7, регулирование CRMP2 было бы потеряно», — сказал Раджиш Кханна.
В исследовании на животных ученые создали пептид из канала, соответствующего этой области связывания, и вставили его в аденоассоциированный вирус, чтобы доставить его в нейроны, где он нарушил бы функцию NaV1.7.
Когда сконструированный вирус вводили мышам с хронической болью, такой как чувствительность к прикосновению, теплу или холоду, и периферической невропатией из-за химиотерапии, для купирования боли у животных требовалось от недели до 10 дней.
Они также измерили его ингибирующие способности на клетках приматов и человека. Команда предупреждает, что требуется дополнительная работа, но они считают, что успех их исследования превратится в терапию для людей.
«Мы нашли способ взять сконструированный вирус, содержащий небольшой фрагмент генетического материала белка, который есть у всех нас, и заразить нейроны для эффективного лечения боли», — сказал Раджиш Кханна. «Мы находимся на пороге важного момента в генной терапии, и это новое применение при хронической боли — лишь последний пример».
Исследование было опубликовано в журнале Proceedings of the Natural Academy of Sciences (PNAS).